Zawartość
- Główna różnica
- Wykres porównania
- Co to są związki jonowe?
- Co to są związki molekularne?
- Związki jonowe vs. związki molekularne
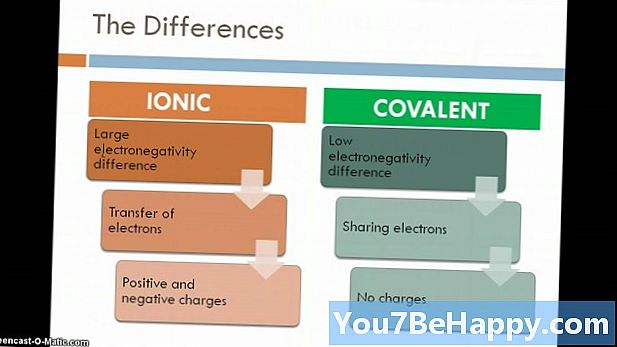
Główna różnica
Związek jest rozpoznawany jako substancja, która powstaje, gdy dwa lub więcej pierwiastków łączy się w określonych proporcjach przez wiązanie chemiczne. Związek jonowy to związek powstały w wyniku siły elektrostatycznej przyciągania między metalami i niemetalami. Zwykle związki jonowe pojawiają się w stanie sprzedanej krystaliczności. Ponadto związki jonowe są dobrymi przewodnikami elektryczności i mają wysokie temperatury topnienia i wrzenia. Z drugiej strony związki molekularne powstają w wyniku podziału elektronów między dwoma niemetalami. W stosunku do związku jonowego są słabym przewodnikiem elektrycznym i mają niską temperaturę topnienia i wrzenia.
Wykres porównania
| Związki jonowe | Związki molekularne | |
| Tworzenie | Związki jonowe powstają w wyniku siły elektrostatycznej przyciągania między metalami i niemetalami. | Związki molekularne powstają w wyniku podziału elektronów między dwoma niemetalami. |
| Grupa | Związki jonowe powstają między metalem a nie-mentalnym. | Związki cząsteczkowe powstają, gdy chemicznie łączą się dwa niemetale |
| Więź | Związek Jonowy powstaje w wyniku siły elektrostatycznej przyciągania znanej jako wiązanie jonowe. | Związki molekularne powstają w wyniku kowalencyjnego wiązania między pierwiastkami. |
| Temperatura topnienia i wrzenia | Wysoki | Niska |
| Stan | Związki jonowe są zawsze w stanie stałym, tworząc krystaliczny wygląd. | Związki molekularne mogą być w dowolnym stanie, w postaci stałej, ciekłej lub gazowej w temperaturze pokojowej. |
| Dyrygent energii elektrycznej | Dobry | Zły |
Co to są związki jonowe?
Związki te powstają w wyniku siły elektrostatycznej przyciągania między metalami i niemetalami. Mówiąc prościej, siła (wiązanie jonowe) powoduje, że dodatnio i ujemnie naładowane reagują razem, tworząc związek. Zazwyczaj związki jonowe pojawiają się w stanie sprzedanej krystaliczności i są dobrymi przewodnikami elektryczności o wysokich temperaturach topnienia i wrzenia. Związki jonowe powstają między metalami i niemetalami i mają jakiś błyszczący wygląd.
Przykład: Sól stołowa (NaCl) jest najczęstszym przykładem związku jonowego. W tej formacji Sód (NA) jest metalem, podczas gdy Chlor (Cl) nie jest metalem, oba są utrzymywane razem ze względu na siłę elektrostatyczną przyciągania między nimi.
Co to są związki molekularne?
Związki powstałe w wyniku podziału elektronów między niemetalami są znane jako związek molekularny. Reagujące tu pierwiastki są utrzymywane razem ze względu na wiązanie kowalencyjne i dlatego związki te często określa się jako związki kowalencyjne.W stosunku do związku jonowego są słabym przewodnikiem elektrycznym i mają niską temperaturę topnienia i wrzenia.
Przykład: W ozonie (O3) tlen łączy się z dzieleniem elektronów, tworząc ozon.
Związki jonowe vs. związki molekularne
- Związki jonowe powstają w wyniku siły elektrostatycznej przyciągania między metalami i niemetalami, natomiast związki cząsteczkowe powstają w wyniku podziału elektronów między dwoma niemetalami.
- Związki molekularne powstają, gdy dwa niemetale chemicznie łączą się, natomiast związki jonowe powstają między metalem a nie-mentalnym.
- Związki molekularne powstają w wyniku wiązania kowalencyjnego między pierwiastkami, natomiast związek jonowy powstaje w wyniku siły przyciągania elektrostatycznego znanej jako wiązanie jonowe.
- Związki molekularne mają niską temperaturę topnienia i wrzenia w porównaniu ze związkami jonowymi.
- Związki molekularne mogą być w dowolnym stanie stałym, ciekłym lub gazowym w temperaturze pokojowej, podczas gdy związki jonowe są zawsze w stanie stałym, tworząc krystaliczny wygląd.
- Związki molekularne są słabym przewodnikiem elektryczności, podczas gdy związki jonowe są dobrym przewodnikiem elektryczności.